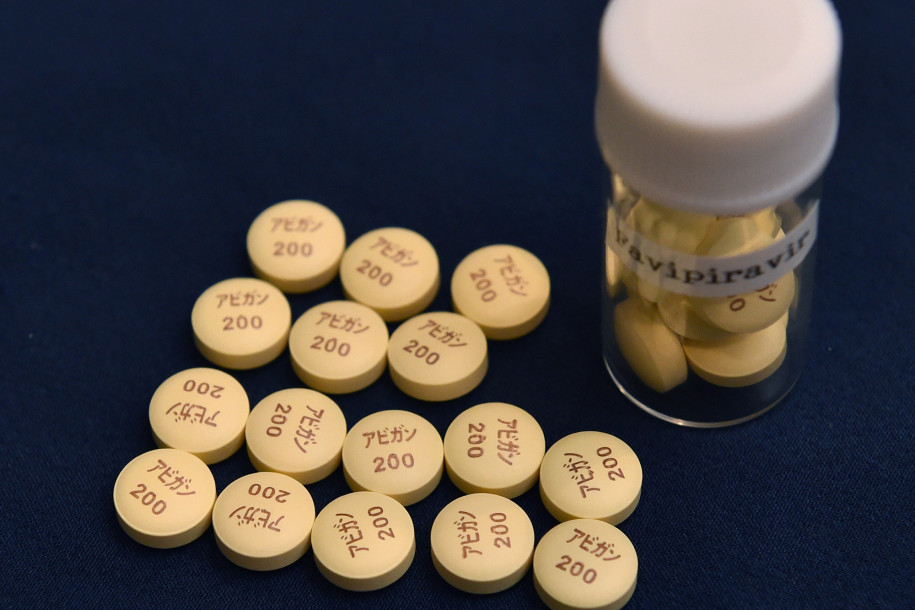
Alle roper på en vaksine eller en medisin som hindrer eller helbreder Covid-19 influensaen. Den kan imidlertid allerede være her, men det norske Statens Legemiddelverk sier nei takk, fordi den ikke har vært igjennom alle de byråkratiske hindre.
Logg inn for å lese videre (abonnenter).
Støtt Norges viktigste uavhengige medium!
Bli abonnentPluss-artikler blir åpnet 48 timer etter publisering. Artikler som er eldre enn to år er forbeholdt abonnenter.